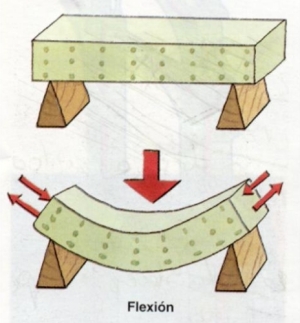
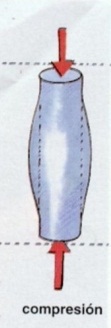
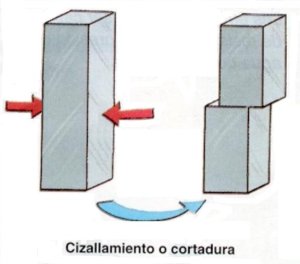
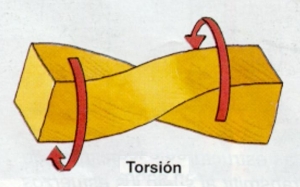
1. GENERALIDADES DE LOS MATERIALES.
Para empezar en este capítulo se estudiarán los temas que conciernen los materiales puros y no puros, enlaces químicos así como también los materiales que son utilizados en la ingeniería.
Para tal fin cabe iniciar en una primera instancia definiendo el término de sustancia: una sustancia es cualquier variedad de materia de composición definida y reconocible. Podemos clasificarlas en:
a) Materiales puros.
b) Materiales no puros.
1.1 Materiales puros.
Las sustancias puras están formadas por partículas (átomos o moléculas) iguales, tienen una composición fija, no pueden separase por medios físicos. Sus propiedades son específicas, bien definidas y no varían, aun cuando dicha sustancia pura se encuentre formando parte de una mezcla.
Algunas de estas propiedades son:
• El color
• El sabor
• El olor
• La densidad
• La temperatura de (fusión y ebullición)
• La solubilidad
• La conductividad térmica y eléctrica.
Es característico de una sustancia pura que la temperatura a la cual sufre un cambio de estado (fusión, ebullición, etc.) permanece constante durante el cambio. Por lo tanto, el punto de congelación de 100g de agua permanece constante a 0ºC desde la congelación del primer gramo hasta la del último.
Como sustancias puras tenemos el cobre, la sal, el diamante, el agua, el azúcar de mesa, el oxígeno, el mercurio, la vitamina C, el ozono, entre muchos otros.

http://quimicaisfd95.wikispaces.com/Tabla+Peri%C3%B3dica
Las sustancias puras a su vez se clasifican en:
a) Elementos.
b) Compuestos.
Ambos son homogéneos ya que mantienen sus propiedades y características.
1.1.1 Elementos: Los elementos son sustancias fundamentales simples, pueden ser moleculares o atómicas, y no se descomponen en otras sustancias distintas. Ejemplo: oxígeno, nitrógeno, nitrógeno gaseoso (N2), la plata (Ag).
1.1.2 Compuestos: Constan de compuestos de elementos y por lo tanto son sustancias más complejas. Un compuesto puede separarse, o descomponerse en sus elementos constituyentes, pero los elementos mismos resisten todos cualquier intento de fragmentación en sustancias más simples y fundamentales.
Están formados por moléculas y éstas están formadas por unión de átomos de distintos elementos. Todas las moléculas del mismo compuesto son iguales entre sí. Es importante saber que los compuestos no son mezclas, no son separables por medios físicos. Además, tienen composiciones fijas características.
Un compuesto se representa a menudo mediante una abreviatura química compuesta de los símbolos de sus elementos. Como por ejemplo: El NaCl representa el cloruro de sodio, y el H2O representa el agua, dióxido de carbono (CO2).
1.2 Materiales no puros (Mezclas).
Es la combinación de dos o más sustancias puras de tal forma que no ocurre una reacción química, cada sustancia mantiene su identidad y propiedades. Si después de mezclar algunas sustancias, no podemos recuperarlas por medios físicos, entonces ha ocurrido una reacción química y las sustancias han perdido su identidad.
Como por ejemplo, La arena con limaduras de hierro, que a simple vista es fácil ver que la arena y el hierro mantienen sus propiedades; la leche, la madera, el concreto, el agua salada, el aire, el granito, el aceite de motor, el chocolate, etc.
Una mezcla puede ser separada en sus componentes (sustancias) simplemente por métodos físicos. Estas pueden ser clasificadas en:
a) Homogéneas.
b) Heterogéneas.
1.2.1 Mezclas Homogéneas: Se denomina comúnmente solución, y consta de una sola fase. Entre las soluciones están el agua salada, la gasolina, el vinagre, el vodka y el aire. Una solución puede ser sólida, líquida o gaseosa, y sus componentes pueden ser elementos o compuestos. No son uniformes; en algunos casos, puede observarse la discontinuidad a simple vista (sal y carbón, agua y aceite, por ejemplo); en otros casos, debe usarse una mayor resolución para observar la discontinuidad.
Se pueden separar por medio de:
• Cristalización
• Destilación Simple
1.2.1.1 Separación de mezclas homogéneas por medio de Cristalización: Esta técnica consiste en hacer que cristalice un soluto sólido con objeto de separarlo del disolvente en el que está disuelto. Para ello es conveniente evaporar parte del disolvente o dejar que el proceso ocurra a temperatura ambiente. Si el enfriamiento es rápido se obtienen cristales pequeños y si es lento se formarán cristales de mayor tamaño.
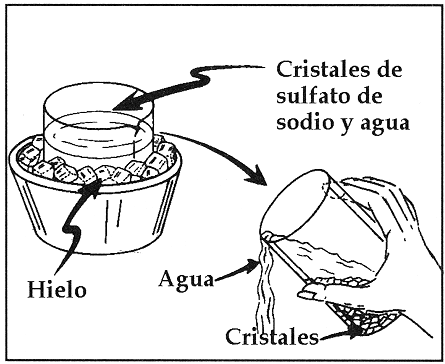
http://www.pps.k12.or.us/district/depts/edmedia/videoteca/curso1/htmlb/SEC_132.HTM
1.2.1.2 Separación de mezclas homogéneas por medio de Destilación: Esta técnica se emplea para separar líquidos de una disolución en función de sus diferentes puntos de ebullición. Es el caso, por ejemplo, de una disolución de dos componentes, uno de los cuáles es volátil (es decir, pasa fácilmente al estado gaseoso). Cuando se hace hervir la disolución contenida en el matraz, el disolvente volátil, que tiene un punto de ebullición menor, se evapora y deja un residuo de soluto no volátil. Para recoger el disolvente así evaporado se hace pasar por un condensador por el que circula agua fría. Ahí se condensa el vapor, que cae en un vaso o en un Erlenmeyer.
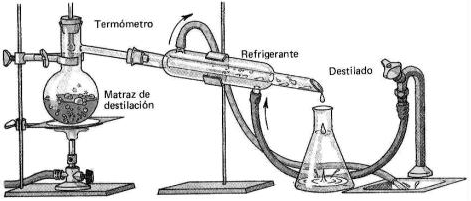 http://www.educarchile.cl/Portal.Base/Web/VerContenido.aspx?ID=106048
http://www.educarchile.cl/Portal.Base/Web/VerContenido.aspx?ID=106048
1.2.2 Mezclas Heterogéneas: Son aquellas cuyo aspecto diferencia una parte de otra, están formadas por dos o más componentes que se distinguen a simple vista y contiene cantidades diferentes de los componentes.
Por ejemplo, mezclas de arena y sal, arena y agua, gasolina y agua, las burbujas de aire y agua, y polvo y aire.
Se pueden separar por medio de:
• Filtración
• Decantación
• Separación Magnética
1.2.2.1 Separación de mezclas heterogéneas por medio de Filtración: Este procedimiento se emplea para separar un líquido de un sólido insoluble.
Ejemplo: Separación de agua con arena. A través de materiales porosos como el papel filtro, algodón o arena se puede separar un sólido que se encuentra suspendido en un líquido. Estos materiales permiten solamente el paso del líquido reteniendo el sólido.
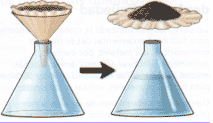
http://www.educared.org/global/anavegar5/podium/images/B/1563/metodos_mecanicos.htm
1.2.2.2 Separación de mezclas heterogéneas por medio de Decantación:
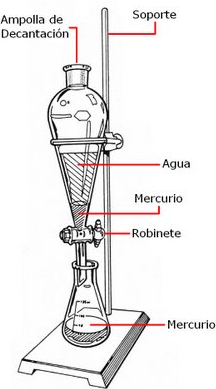
Esta técnica se emplea para separar 2 líquidos no miscibles entre sí. Ejemplo: Agua y aceite.
La decantación se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba (si queremos tomar el componente menos denso) o por abajo (si queremos tomar el más denso).
En la separación de dos líquidos no miscibles, como el agua y el aceite, se utiliza un embudo de decantación que consiste en un recipiente transparente provisto de una llave en su parte inferior. Al abrir la llave, pasa primero el líquido de mayor densidad y cuando éste se ha agotado se impide el paso del otro líquido cerrando la llave. La superficie de separación entre ambos líquidos se observa en el tubo estrecho de goteo. http://fraymachete-fq.blogspot.com/2008_11_01_archive.html
1.2.2.3 Separación de mezclas heterogéneas por medio de separación magnética: Esta técnica sirve para separar sustancias magnéticas de otras que no lo son. Al aproximar a la mezcla el imán, éste atrae a las limaduras de hierro, que se separan así del resto de la mezcla.

http://funfairizpisua.blogspot.com/2010_12_01_archive.html
1.3 Enlaces Químicos.
Para tener una mejor visión y conceptualización de la tabla periódica y los enlaces químicos, es importante conocer conceptos básicos como son por ejemplo las definiciones de qué es un átomo, una molécula, un elemento químico, una sustancia pura, una mezcla, un enlace químico, un metal, un no metal o metaloide, etc.
Es por esto que se comenzara explicando dichos conceptos básicos requeridos para el estudio de los enlaces químicos.
1.3.1 Átomo:
El átomo de un elemento es la cantidad más pequeña de este cuerpo, que puede contribuir a la formación de una molécula. Es considerado el componente básico de toda la materia, poseen un núcleo, protones y neutrones rodeado por electrones.
Los átomos de diferentes elementos tienen diferente número de protones, el átomo más simple es el hidrógeno, qué está compuesto por un electrón y un protón.
Hacer click en el link: http://www.youtube.com/watch?v=0WnjSm-Mg1Q&feature=related
1.3.2 Molécula: Está formado por grupos de átomos unidos que forman conjuntos llamados moléculas, los átomos que se encuentran en una molécula se mantienen unidos debido a que comparten o intercambian electrones.
Las moléculas están hechas de átomos de uno o más elementos, algunas moléculas están hechas de un solo tipo de átomo, por ejemplo dos átomos de oxigeno se unen para formar una molécula de O2, o un átomo de nitrógeno se une con tres átomos de hidrogeno y forman una molécula llamada NH3.
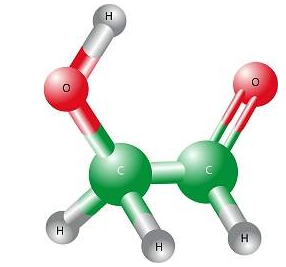
http://www.inovacaotecnologica.com.br/noticias/noticia.php?artigo=molecula-essencial-a-vida-e-encontrada-a-26-000-anos-luz-da-terra&id=010130081210
1.3.3 Especie química: Las especies o individuos químicos son sustancias cuya composición no sufre alteración por medio de los cambios de estado, el agua por ejemplo, puede solidificarse o evaporarse, pero conservará siempre la misma composición química. Diremos por lo tanto, que el agua es una sustancia homogénea y una especie química.
1.3.4 Elementos químicos: Un elemento químico es un tipo de materia, constituida por átomos de la misma clase, compuesto por un número de protones en su núcleo que lo hace pertenecer a una categoría única clasificada con el “número atómico”.
Un elemento químico también es una sustancia que no puede ser descompuesta por una reacción química, en otras más simples; está clasificado en una tabla, llamada “tabla periódica”, clasificada por diferentes propiedades y características, similitudes y diferencias entre los elementos existentes conocidos.
1.3.5 Clasificación de los elementos químicos: A medida que se fueron descubriendo los elementos químicos, se observaron propiedades semejantes entre algunos de ellos, por lo que se les clasifico en dos grandes grupos: metales y no metales (o metaloides).
El sistema periódico de los elementos o mejor dicho el sistema de periodos de los elementos de mendeleiev consiste en la ordenación de éstos en varias filas horizontales y columnas verticales según el orden creciente de sus masas atómicas. Esta clasificación permitió que su autor concibiera la existencia en la naturaleza de algunos elementos hasta entonces desconocidos, así como sus principales propiedades químicas y físicas.
1.3.6 Propiedades físicas y químicas de los elementos:
1.3.6.1 Símbolo: Todos los elementos tienen un símbolo, el símbolo atómico de un elemento sirve para representarlo y consta de una letra mayúscula y una, dos o ninguna minúscula que provienen de su nombre o su nombre en latín, por ejemplo el símbolo del hierro es Fe que proviene de su nombre en latín Ferrum.
http://tablaperiodica1.blogspot.com/2010/07/escandio-elemento-quimico.html
1.3.6.2 Masa atómica: La masa atómica es la masa del átomo de un elemento, expresada en unidades de masa atómica. Es casi igual al número de protones más el número de neutrones de su núcleo, esto es así por que los protones como los neutrones tienen una masa prácticamente igual a una y la masa de los electrones es demasiado pequeña por lo tanto insignificante.
1.3.6.3 Número atómico: Es el número total de protones en el núcleo de un átomo
Este número diferencia a un elemento de los demás, es también igual a la cantidad de electrones de un átomo neutro del elemento. Por ejemplo el Actinio (Ac) tiene número atómico 89, Esto quiere decir que el actinio tiene 89 protones en su núcleo.
http://tablaperiodica1.blogspot.com/2010/07/escandio-elemento-quimico.html
1.3.6.3 Número de neutrones (isotopos): El número de neutrones de un átomo es igual a la masa atómica del átomo redondeada al número entero más próximo (número másico) menos el número de protones. Esto se debe a que protones y neutrones tienen una masa atómica aproximada de 1 u.m.a, puesto que los elementos tienen más de un isotopo.
El número de neutrones que está plasmado en la tabla periódica se refiere al isótopo más abundante del elemento.
Ejemplo: El boro (B) tiene una masa atómica de 10.81 y número atómico de 5. Al redondear 10.81 al entero más próximo sale 11. Restando de este número 11 el número de protones (o número atómico) se obtiene 6, que indica que el isótopo más abundante del boro tiene 6 neutrones.
1.3.6.4 Estructura o configuración electrónica: Corresponde a la configuración o estructura electrónica del estado fundamental: configuración más estable y más probable.
En la tabla entre corchetes se indica la estructura del gas noble anterior al elemento que corresponde a su estructura electrónica interna y, a continuación, los electrones más externos que lo diferencian de dicho gas noble. En algunos casos se presentan anomalías.
La tabla I contiene las estructuras electrónicas por subniveles de todos los elementos hasta el 118. Además, existe una tabla para ver la relación entre llenado de los orbitales y situación en la tabla.
1.3.6.5 Electrones en los niveles de energía: Se da el número total de electrones en las distintas capas, (K,L,M,N,P,O,Q), o niveles energéticos (1,2,3,4,5,6,7) del átomo en estado fundamental.
1.3.6.6 Número de oxidación: En esta parte de la tabla se muestran el número de oxidación del elemento. En el caso de poseer varios se da en negrita el más importante. El número de oxidación de un átomo en un compuesto es el número de electrones ganados o perdidos por dicho átomo con respecto al mismo átomo aislado. Está relacionado con la estructura electrónica del elemento.
1.3.6.7 Electronegatividad: Es la tendencia que tiene un átomo de atraer hacia sí los electrones de su enlace con otro átomo. La diferencia de electronegatividad de entre los átomos que se unen, puede servir para establecer el tipo de enlace entre ellos.
La electronegatividad está relacionada con la afinidad electrónica y la energía de ionización del elemento, de forma a que si el elemento tiene altos valores de ambas, tiene entonces alta electronegatividad y es no metal.
1.3.6.8 Energía o potencial de ionización: La primera energía de ionización es la energía necesaria para arrancar un electrón a un átomo en estado gaseoso y transformarlo en un ion mono positivo.
Valores altos indican carácter no metálico del elemento.
Los factores de que depende el potencial de ionización son:
1. La distancia al núcleo del electrón que se pierde
2. La carga del núcleo
3. El efecto pantalla de los electrones subyacentes
4. La proximidad de la estructura externa del átomo a las de los gases nobles.
1.3.6.9 Afinidad electrónica o electroafinidad: Es la energía que suministrada cuando un átomo gaseoso en su estado fundamental capta un electrón y se transforma en un ion negativo. Es una magnitud difícil de medir y en muchos casos no se conoce el valor exacto. Los valores positivos indican que cuando el átomo gaseoso gana un electrón, se desprende energía. Los valores negativos quieren decir que hay que suministrar energía para que el átomo gaseoso gane el electrón.
Valores altos indican carácter no metálico del elemento.
1.3.6.10 Radio atómico: Es la mitad de la distancia entre los centros de dos átomos contiguos del elemento. En el caso de los metales se utiliza la distancia entre los centros de dos átomos en una muestra sólida. En el caso de los no metales se utiliza la distancia entre los centros de dos átomos unidos por enlace químico y se denomina también como radio covalente.
El radio atómico aumenta en un grupo y disminuye en un periodo al aumentar el número atómico.
1.3.6.11 Número de valencia: Es una medida de la cantidad de enlaces químicos formados por los átomos de un elemento.