EQUILIBRIO QUIMICO—RESUMEN JULIO 31 DE 2009…TUVIMOS LECCION SOBRE VELOCIDAD Y CONSTANTE DE VELOCIDAD
Jul 31
2009
Modificaciones del equilibrio
El estado de equilibrio para un sistema químico está caracterizado por unas concentraciones o presiones parciales de reactivos y productos que permanecen inalteradas en el tiempo. Las concentraciones o presiones de equilibrio dependen de los valores iniciales y de la temperatura. Sin embargo, los equilibrios químicos son dinámicos y, por tanto, un cambio en las condiciones que los hacen posibles determina unas nuevas condiciones de equilibrio.
Principio de Le Chatelier
Cuando un sistema químico está en equilibrio (Q = K) (ver t13) y se le somete a una perturbación, el sistema evoluciona espontáneamente hacia un nuevo estado de equilibrio, que se caracteriza por unas concentraciones de reactivos y productos que cumplen la condición de equilibrio Q = K.
Existen tres variables que afectan al estado de equilibrio:
* Cambios en la concentración de las especies reaccionantes.
* Cambios en la presión y el volumen.
* Efecto de la temperatura.
La constante de equilibrio permite analizar cuantitativamente las alteraciones del estado de equilibrio; sin embargo, muchas veces no se dispone de información suficiente para llevar a cabo cálculos cuantitativos, por lo que es necesario un análisis cualitativo de la respuesta de un sistema ante una perturbación.
El principio de Le Chatelier es una herramienta cualitativa que indica la dirección del desplazamiento del equilibrio. Establece que «un cambio o perturbación en cualquiera de las variables que determinan el estado de equilibrio de un sistema químico, produce un desplazamiento del equilibrio en el sentido de contrarrestar o minimizar el efecto causado por la perturbación».
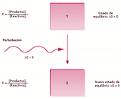
Cambios en las concentraciones de las especies reaccionantes
![]()
El cociente de reacción es:
![]()
Si se añade hidrógeno, Q Kc.
Cambios en la presión y el volumen
Para una reacción química cualquiera, un aumento de la presión (o disminución del volumen) provoca un desplazamiento del equilibrio en el sentido en el que se produce un menor número de moles de gas.
Una reducción de la presión (o un aumento del volumen) desplaza el equilibrio en el sentido en el que se produce un mayor número de moles de gas.
Los cambios de presión no afectan al equilibrio cuando Dn = 0, ya que, en este caso, el número de moles gaseosos a ambos lados de la ecuación es idéntico.
En las reacciones químicas en las que sólo participan sólidos y líquidos, los cambios de presión casi no afectan al estado de equilibrio, puesto que sólidos y líquidos son prácticamente incompresibles.
Tags: resumen clases
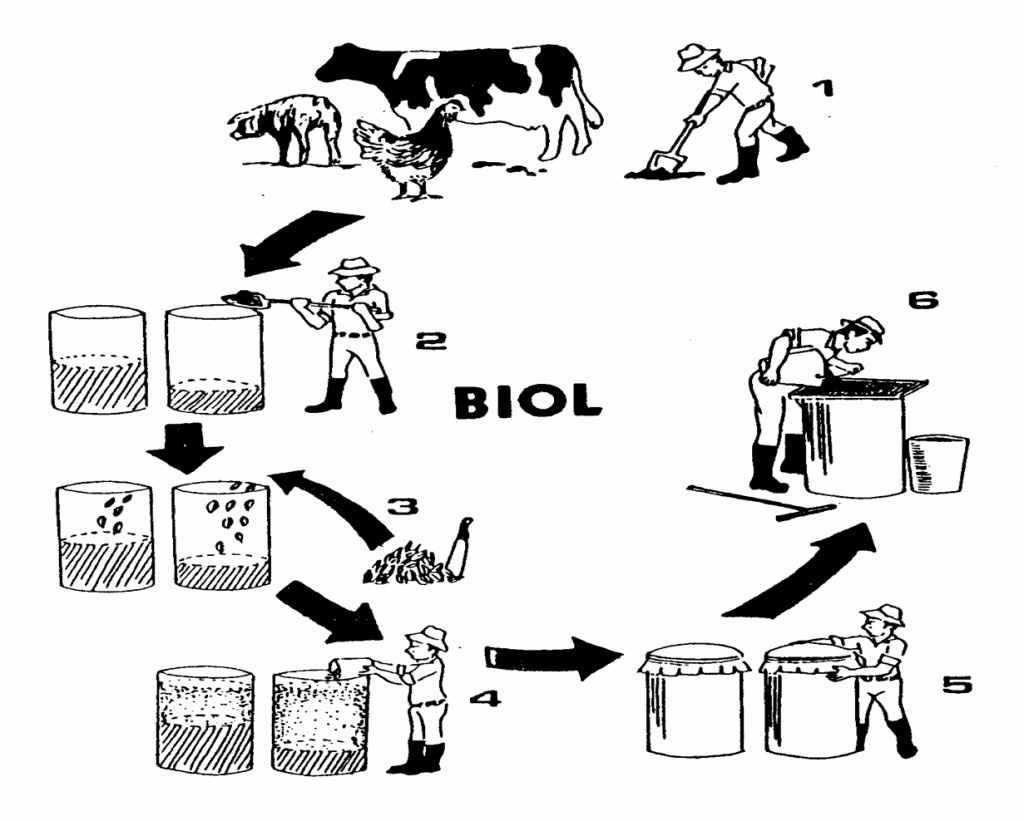
BIOL
Se obtiene del proceso de descomposición anaeróbica de los desechos orgánicos.. En un biodigestor
El Biol es el liquido que se descarga de un digestor y sirve como abono foliar, fuente orgánica de fitoreguladores que estimulan el desarrollo de las plantas.
PRODUCCIÓN DEL BIOL
MATERIALES
Estiércol (de ganado, porcino o gallinaza)
Tanques digestores
Machete, pala, baldes
Alfalfa o leguminosa picada
Plástico u otro cobertor
Mallas
Pasos para la preparación
Recolectar el estiércol
Poner en un tanque la mitad del estiércol y en el orto la cuarta parte
Poner la leguminosa picada
Llenar los tanques con agua y sellar los tanques herméticamente y dejar fermentar por 90 días
Filtrar el biol
USO DEL BIOL
AL FOLLAJE
AL SUELO
A LA SEMILLA
A LAS PLANTULAS
EN BULBOS
“VIVENCIAS DEL CURSO DE VERANO EN CIENCIA POLAR,
Jul 31
2009
 “VIVENCIAS DEL CURSO DE VERANO EN CIENCIA POLAR,
“VIVENCIAS DEL CURSO DE VERANO EN CIENCIA POLAR,
UNIVERSITY CENTRE IN SVALBARD (NORUEGA), 2009.
41ma Mesa de Diálogo
Lugar: Sala de Sesiones ICQA (2do Piso Alto)
Día: Miércoles 29 de Julio de 2009
Hora: 11:30; Finalización: 12:30
Repetición:
Día: Viernes 31 de Julio de 2009
Hora: 09:30; Finalización: 10:30
Lugar: CC. BB. Aula BA11
TÓPICO:
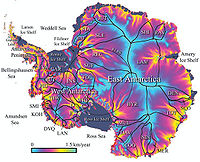
Vivencias del Curso de Verano en Ciencia Polar, University Centre in Svalbard (Noruega)
Instructor: Bióloga Nadia Ordoñez Román
Facilitador: Ph. D. V. A. Riofrío T. (-ICQA-
GRACIAS NADIA…..HEMOS APRENDIDO MUCHAS COSAS…
Ecuador tiene el buque Orion que a realizado trabajos de investigación en la estación cientifica Pedro Vicente Maldonado.

41 MESA DE DIALOGO
“VIVENCIAS DEL CURSO DE VERANO EN CIENCIA POLAR,
UNIVERSITY CENTRE IN SVALBARD (NORUEGA), 2009.
ANDREA PILAR ROMERO
Nadia estudio Biologia en la ESPOL donde se encuentra ahora en su proceso de graduación, ella es una joven, guapa, inteligente y emprendedora, estuvimos escuchando sus experiencias en su curso de verano en el artico donde aprendio bastante:
De lo que mas me llamo la atención:
• Hay 2000 personas en la ciudad y hay 3000 osos polares que aunque son hermosos son muy peligrosos, hay algunas técnicas de seguridad entre ellas el uso de armas que emiten luces de bengala para ahuyentarlos y en ultimo de los casos se usa el rifle, cosa que no es tan recomendable ya que los osos polares están protegidos.
• Hay también renos que migran según la estación del año donde en verano hay luz solar todas las 24 horas y en invierno oscuridad total por el mismo tiempo, las poblaciones nativas van siguiendo a los renos alimentándose de ellos y fabricando su ropa y demás implementos de ellos, se dice que los cambio climaticos afectara primero a este tipo de población ya que los polos serán los primeros en sentir los cambios.
• Es importante compartir los conocimientos con otras personas, esos nos dara oportunidades de crecer intelectualmente y nos ayudara a desarrollar algunas otras actitudes de liderazgo.
• Las oportunidades de aprender se presentan siempre, pero debemos estar preparados.
• El segundo idioma es muy importante es este tiempo donde todo es mas competitivo debemos adquirir capacidades que nos mantengan al dia y actualizados con los requerimientos y los avances del mundo moderno y educativo.









0